Streptokokk gruppe A-infeksjon – håndbok for helsepersonell
Sist endret
Streptokokk A-infeksjon er en av de vanligste årsaker til bakterieinfeksjon hos mennesker, hyppigst i hals og hud. Bakterien forekommer normalt på hud og i svelget uten å forårsake plager, men i sjeldne tilfeller kan det oppstå livstruende infeksjon.
Om streptokokk gruppe A-infeksjon
Streptokokk A-infeksjon forårsakes hovedsakelig av bakteriearten Streptococcus pyogenes. Bakterien kalles på norsk også (beta-hemolytiske) serogruppe A-streptokokker, ofte forkortet til GAS. Betegnelsen hemolytisk kommer av at bakterien danner stoffer som har evnen til å løse opp røde blodceller i dyrkningsmediet i laboratoriet, men denne egenskapen er ikke årsak til de symptomene som infeksjonen fremkaller.
GAS forekommer i Norge vanligvis som lokaliserte, ikke-invasive infeksjoner som tonsillitt (halsbetennelse), impetigo (brennkopper), erysipelas (rosen), otitt (ørebetennelse) og skarlagensfeber. Immunologiske senkomplikasjoner som revmatisk feber (giktfeber) og akutt glomerulonefritt er i dag sjelden i Norge, men er et betydelig problem i mange lavinnkomstland. GAS-infeksjoner har en utpreget sesongvariasjon med toppunkt etter årsskiftet. Dette gjelder både invasive og ikke-invasive tilfeller. Mindre, lokale GAS-epidemier kan ofte sees på vinteren. Alvorlig, invasiv sykdom forekommer hyppigst hos eldre, men alle aldersgrupper kan rammes. Tilfeller av alvorlig GAS-sykdom er i all hovedsak sporadiske tilfeller, men i sjeldne tilfeller kan man se geografiske opphopninger.
Arten Streptococcus pyogenes har gruppe A-polysakkarid i sin cellevegg. Den viktigste virulensfaktoren er det såkalte M-proteinet (kodet av emm-genet), som sitter på bakteriens overflate, og hemmer fagocytose. GAS kan deles inn i minst 120 ulike M-typer, og enda flere emm-gen-typer. GAS kan i tillegg produsere flere ulike toksiner som spiller en rolle for utvikling av symptomer og infeksjonens alvorlighetsgrad.
Beta-hemolytiske streptokokker av gruppe C og G kan gi liknende sykdomsbilder som gruppe A- streptokokker.
Historisk bakgrunn
Det karakteristiske syndromet skarlagensfeber har sannsynligvis vært kjent fra oldtiden. Streptokokker ble første gang funnet mikroskopisk beskrevet ved endokarditt i Norge i 1869. Streptokokker ble i 1874 påvist i erysipelas og fra et tilfelle av barselfeber i 1879. Dyrkning av kokker i kjeder fra erysipelas ble utført i 1883, disse fikk i 1884 navnet Streptococcus pyogenes. Sammenhengen mellom akutt revmatisk feber og streptokokkinfeksjon ble erkjent i 1899. I 1923 ble det oppdaget at skarlagensfeber skyldtes hemolytiske streptokokker. Gruppebestemmelse av streptokokker ble innført i 1933, metoden baserte seg på ulike polysakkarider i bakterienes cellevegg. Dette førte til at man oppdaget at ulike serogruppe var årsak til ulike sykdommer. Sammenhengen mellom akutt glomerulonefritt og streptokokkinfeksjon ble endelig anerkjent i 1941.
Norge
På slutten av 1800-tallet var infeksjoner med gruppe A-streptokokker en av de vanligste dødsårsakene i Norge, spesielt blant barn og hos kvinner som nylig hadde født. Epidemier med skarlagensfeber og sårinfeksjoner var vanlig, og komplikasjoner som giktfeber og streptokokknefritt forekom ofte. I kjølvannet av bedre levestandard og hygiene, samt introduksjon av antibiotika falt dødeligheten. Utbrudd av skarlagensfeber har gjennom tidene vist seg å ha sterkt varierende alvorlighet. I Norge opptrådte skarlagensfeber på hele 1800-tallet som stadige utbrudd med dødelighet på opptil 10%. Skarlagensfeber var den gang en fryktet sykdom og de syke ble holdt i streng isolasjon. Fra slutten av 1800-tallet sank dødeligheten av skarlagensfeber betydelig i Norge og i mange andre vestlige land uten at man kjenner årsaken til dette.
Utbrudd av halsbetennelse og skarlagensfeber var forholdsvis vanlig før pasteurisering av melk, og det er beskrevet flere utbrudd av skarlagensfeber i Norge hvor smittekilden har vært forurenset melk. Bakterien var tidligere årsak til alvorlige, invasive infeksjoner med høy dødelighet, f.eks. den klassiske barselfeberen. I preantibiotisk tid var dødeligheten av GAS-bakteriemi nær 80%. Under annen verdenskrig var det i Norge utbrudd av skarlagensfeber og et noe mindre utbrudd forekom tidlig på 1960-tallet. Deretter roet situasjonen seg betydelig. Skarlagensfeber forekom svært sjeldent, og alvorlige invasive sykdomstilfeller var uvanlig.
Dagens situasjon
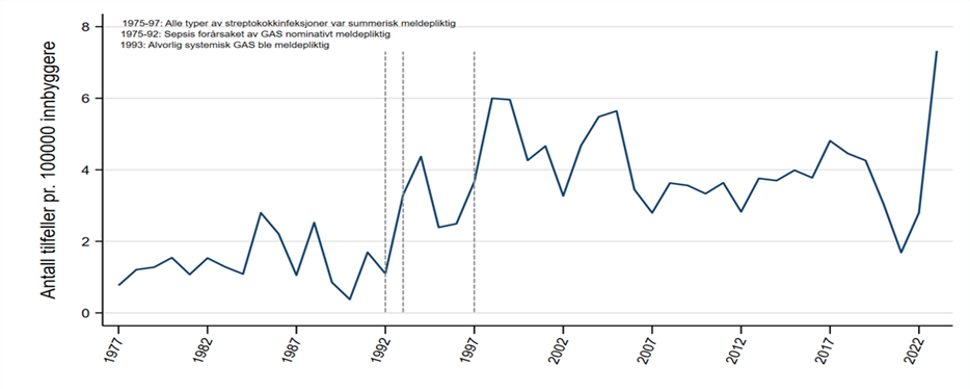
I mange vestlige land så man en endret epidemiologi av GAS fra midt på 1980-tallet. Dette gjaldt også Norge, der økt forekomst og alvorlighet ble observert i 1984-85 og særlig 1987-88. Aldersfordelingen endret seg også med høyere forekomst i alle aldersgrupper og tilkomst av alvorlige tilfeller hos unge voksne, som i tiårene før meget sjeldent ble rammet. Studier viste at serotype M1 (svarer til emm1–gen) GAS endret seg med opptak av nye virulensfaktorer fra midt på 1980-tallet. Antall rapporterte systemiske GAS-infeksjoner falt mye allerede i 1989 og var rolig til 1993. Fra 1993 og fram til 2005 var det en økning av alvorlige invasive og systemiske GAS-tilfeller i Norge (Figur 3) og i mange andre land.
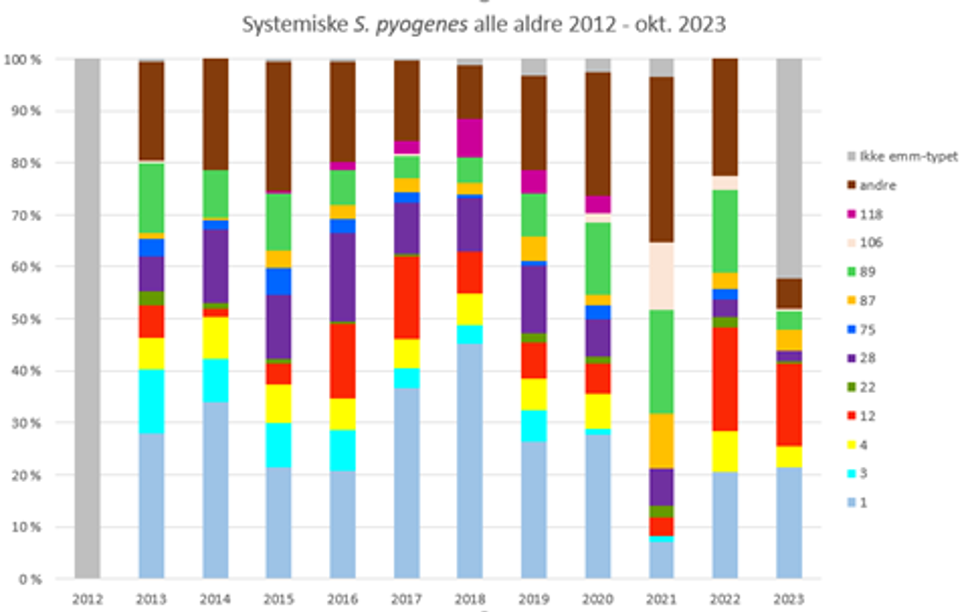
M1/emm1 utgjør fortsatt en stor andel av systemiske isolater. Eldre kunnskap tilsier at enkelte M-typer har sterkere assosiasjon til halsinfeksjon og giktfeber (M1, 3, 6, 14, 18, 19 og 24) sammenliknet med hudinfeksjoner og glomerulonefritt (M2, 49, 57, 59, 60, 61). Bortsett fra emm1, ses disse typene ikke så ofte lenger (Figur 4 og 5 under) Nyere studier viser at emm3 har vært knyttet til epidemier av skarlagensfeber. I Norge har vi ikke oversikt over emm-typer ved skarlagensfeber da diagnosen ikke er meldingspliktig til MSIS. Blant barn med invasive GAS er det en relativ økning av emm12 og en minking av emm4sammenliknet med før pandemien, men tallene er små, og estimatene dermed usikre.
Data fra NORM/NORM-vet 2022 viser at alle invasive GAS stammer var følsomme for penicillin. Under pandemien var det imidlertid en økning i resistens mot erytromycin (ca 20% i 2021) og klindamycin (ca. 10% i 2021), samt mot tetracyclin (ca. 40% i 2021). NORM-rapporten for 2022 påpeker at dette er betinget av noen få isolater av emm22 og emm106 som var svært resistente og som prosentvis utgjorde en stor andel fordi totaltallet var lavt under pandemien. I 2022 var tallene nede på pre-covid19 nivåer igjen: erytromycin (6.5%), klindamycin (4.1%) og tetracyclin (17.1%).
Mindre lokale opphopninger eller utbrudd forekommer forholdsvis sjeldent, men er rapportert fra ulike deler av verden. I 2016-17 var det et større utbrudd av invasiv sykdom i Ontario, Canada med mer enn 132 tilfeller hvorav 9 dødsfall.
I desember 2022 ble det rapportert om økt forekomst av invasive GAS-infeksjoner (iGAS) hos barn under 10 år i flere land i Europa. En sikker økning i antall invasive GAS-tilfeller var da ikke registrert i Norge. Men vinteren 2023 fikk FHI meldt flere invasive GAS-infeksjoner til MSIS enn det som ble meldt i årene før covid-19 pandemien. Økningen var tydeligst etter nyttår og blant barn under 10 år. Det ble også rapportert perioder med økt forekomst av invasive GAS-infeksjoner hos voksne og eldre vinteren 2023 sammenlignet med årene før covid-19 pandemien. Forekomsten var på topp i mars og har siden blitt mer normalisert, selv om det fortsatt var noe forhøyet forekomst frem til sommeren 2023, særlig hos de yngste aldersgruppene. Fra juli ser det ut til at forekomsten ligner på tidligere år, selv om det totalt sett fortsatt lå noe høyt høsten 2023.
Fra desember 2023 fikk FHI meldt flere iGAS hos voksne og særlig hos de over 70 år sammenlignet med sesonger før pandemien. Fra slutten av januar 2024 ble det også rapportert en økning hos barn under 10 år. Tilsvarende funn er rapportert fra bl.a. Sverige, Danmark og England. FHI har publisert overvåkingsdata fra MSIS for perioden med økt forekomst av iGAS fra desember 2022 til våren 2024 (eurosurveillance.com). Tilfellene toppet seg i januar og februar 2024, særlig hos barn under 10 år og eldre over 70 år. I mars og april 2024 har antallet tilfeller gått ned, og i mai ser det ut til at forekomsten har normalisert seg. FHI har også laget en nyhetssak om dette.
Blant de invasive GAS stammene som er undersøkt, er det ikke funnet noen nye typer, og alle har vært følsomme for penicillin.
FHI publiserer oppdatert data for forekomst av iGAS i høysesong i Ukerapporter om covid-19, influensa og andre luftveisinfeksjoner.
Forekomsten av infeksjonssykdommer har vært lavere under pandemien, og immunforsvaret har ikke fått trent seg like godt på å bekjempe infeksjoner. Det kan ha ført til lavere spesifikk immunitet i befolkningen mot noen smittestoffer. Denne «immunologiske gjelden» kan komme til uttrykk som økt forekomst av virusinfeksjoner, men sannsynligvis også bakterieinfeksjoner som GAS. Det er i tillegg generelt høyere risiko for alvorlige bakterielle infeksjoner etter en virusinfeksjon som vannkopper eller influensa.
For mer detaljer om antall meldte tilfeller i Norge, se avsnitt lenger ned under "Forekomst i Norge".
Bærerskap
Normalt finnes bakterien i tonsillofarynks hos mye mindre enn 10% av befolkningen. Andelen bærere i befolkningen varierer med alder (mest hos barnehagebarn og i tidlig skolealder), med årstid (mest om vinteren) og med den epidemiologiske situasjonen som kan variere fra år til år, også lokalt. Ved utbrudd i barnehager har man sett over 50% bærere hos barnehagebarn.
Personale med langvarige hudlesjoner (psoriasis, eksem) kan bli langvarig GAS-bærere i lesjonene sine og særlig i sykehus gi opphav til infeksjoner. Det er også beskrevet fødselshjelpere som har gitt opphav til flere tilfeller av GAS-barselfeber. I slike situasjoner kan intermitterende rektalbærerskap forekomme.
Smittemåte
Ved øvre luftveisinfeksjon foregår smitte ved nærdråpesmitte og kontakt, direkte og indirekte. Trange boforhold og tett omgang i miljøer som militærleirer og barnehager fremmer nærdråpesmitte. Det er vist at GAS kan overleve flere uker i støv i sengetøy o.l., men dette spiller relativt liten rolle som smittespredning blant friske. I institusjoner med individer som har lavere motstandskraft kan slik smittespredning ha betydning. Tilsøling med luftveissekret kan føre til at GAS kan overføres via leker. Rhinitt øker smitterisikoen. Pasienter med tonsillitt er vanligvis smitteførende 10-20 dager i ubehandlede og ukompliserte tilfeller. Antibiotikabehandlede tonsillitter har sterkt fall i smittsomhet allerede etter ett døgn. Hudinfeksjon smitter ved direkte og indirekte kontakt via hudbæring på frisk hud. Overføring gjennom næringsmidler som er kontaminert av personer som har håndtert matvarer var vanlig før og kan i sjeldne tilfeller forekomme også i dag. I forbindelse med noen tilfeller av nekrotiserende fasciitt har det også vært mistenkt inokulering ved injeksjoner eller annen hudlesjoner.
Inkubasjonstid
Kort, vanligvis 1-3 døgn. Ved impetigo blir pasientene først bærere av GAS på hel hud, deretter kan impetigo utvikles etter 10-14 dager. Invasiv sykdom kan variere mht. inkubasjonstid. GAS kan invadere i forbindelse med en akutt tilstand som øvre luftveisinfeksjon. Andre invasive tilstander kan skyldes introduksjon i dypere vev gjennom en lesjon fra en bærertilstand hos individet selv som kan ha vart i noe tid.
Symptomer og forløp
Det vanligste sykdomsbildet er ukomplisert faryngitt og tonsillitt, dernest hudinfeksjoner. Det antas at 10-30% av alle tonsillitter skyldes GAS, men dette varierer mye med årstid, alder og epidemiologisk situasjon. Eksponering for bakterien kan føre til en bærertilstand, eller til lokalisert eller invasiv infeksjon. Klinisk kan GAS-infeksjon deles inn i flere hovedgrupper, men disse kan ofte overlappe:
Ikke-invasive infeksjoner
I øvre luftveier faryngitt, tonsillitt (med eller uten skarlagensfeber, sinusitt, rhinitt og otitt). I hud vanlige brennkopper (impetigo) og den sjeldnere ulcerøs impetigo (ektyma).
Skarlagensfeber forårsakes av spesifikke toksiner produsert av streptokokkbakterien og immunresponsen på disse toksinene. De vanligste første symptomene på skarlagensfeber er akutt debut med feber, halssmerter, belagte tonsiller og rød munnslimhinne (enantem), hodepine, kvalme og oppkast etterfulgt av finprikket, “sandpapiraktig”, rødt utslett etter 12-48 timer som ofte starter på bryst- og magepartier I tillegg diffust, småprikkete rødt utslett i ansiktet unntatt området rundt munnen, som ofte virker ekstra blekt. Utslettet spres perifert og når sin maksimale utbredelse og rødme i løpet av to døgn, og forsvinner etter 4-5 døgn. Rød, nuppete tunge (såkalt bringebær- eller jordbærtunge) er karakteristisk for sykdommen, og ses gjerne etter noen døgn. Etter 1-2 uker etter sykdomsstart ser man ofte hudavskallinger på de steder hvor utslettet har vært mest markert som på hender og føtter. Komplikasjoner kan være bl.a. ørebetennelse, bihulebetennelse, peritonsillitt og lungebetennelse. Tegn på skarlagensfeber kan også ses ved sårinfeksjon og barselfeber. Det er sjelden man får skarlagensfeber mer enn én gang, og sykdommen betraktes vanligvis som en barnesykdom.
Matsmitte kan i sjeldne tilfeller forårsakes av GAS-bakterien og andre grupper av streptokokkbakterien. Smittekilden er vanligvis en person med halsonde eller håndinfeksjon som håndterer næringsmidler og forurenser disse gjennom dårlig hygiene. Vanligste næringsmidler er melk, iskrem, egg og salater som har stått i romtemperatur i lengre tid. Utbrudd er globalt beskrevet i militærleire, sykehjem og fengsler. Symptomer ved slik matforgiftning er vanligvis øvre luftveisinfeksjoner som faryngitt eller tonsilitt.
Lokaliserte invasive tilstander
Lokalisert invasiv infeksjon i øvre luftveier kan gi betennelse i ørebensknuten (mastoiditt) og peritonsillær abscess. Lokalisert invasiv infeksjon i huden kan gi rosen (erysipelas), akutt lymfangitt, abscesser og cellulitter (diffus bløtvevsinfeksjon uten nekrose). Barselfeber er en oppadstigende uterininfeksjon etter fødsel, og kan ha mange årsaker. Særlig alvorlig er barselfeber forårsaket av GAS.
Nekrotiserende fasciitt er en dypere infeksjon med nekrose i underhuden ned mot muskelfascien. I dette vevet kan infeksjonen bre seg raskt videre horisontalt i tilgrensende vev. Etter hvert brer prosessen seg også oppover mot overhud med misfarging, ødem og bullae. Man kan også se noe muskelskade. Nekrotiserende fasciitt har oftest en svær systemisk toksisk komponent som ved sepsis. I motsetning til ved andre hudmanifestasjoner ved GAS (spesielt erysipelas og cellulitt), finner man ved nekrotiserende fasciitt ofte beskjedne overflatiske funn, men med påfallende kraftig lokal smerte.
Andre lokaliserte invasive tilstander kan være pneumoni og empyem, postoperative sårinfeksjoner, primær peritonitt, artritt og osteomyelitt.
Systemisk (invasiv) sykdom
Systemisk invasiv sykdom kan gi bakteriemi, sepsis og/eller meningitt, og sjeldnere akutt endokarditt og perikarditt. Sykdomsforløpet kan være svært akutt. Invasive GAS-tilstander kan – som sepsis med andre agens – starte med uspesifikke, influensaliknende symptomer. Abdominalsymptomer kan være første symptom. Tilstanden kan raskt utvikle seg til sepsis med flerorgansvikt, septisk sjokk og død hos tidligere friske personer i alle aldre.
Streptokokk toksisk sjokksyndrom (STSS) er en nærmere definert variant av septisk sjokk med tidlig organsvikt som første gang ble beskrevet i 1993.
Lemierres syndrom kan utvikles etter en halsbetennelse forårsaket av bakterier i streptokokkfamilien. I krater og groper på tonsillene som er skapt av streptokokkinfeksjonen kan det utvikles anarobe bakterier, mest vanlig er Fusobacterium necrophorum. Syndromet ble beskrevet første gang i 1936 og er kjennetegnet ved en livstruende sepsis med spredning til blant annet lunger. Syndromet er sjeldent, men kan ses spesielt hos tidligere frisk unge i 10-30-årsalderen etter en halsbetennelse.
Immunologiske senkomplikasjoner
Akutt poststreptokokk glomerulonefritt opptrer gjerne 1-3 uker etter en halsinfeksjon eller impetigo. Klassiske symptomer er allmennsymptomer med feber og magesmerter, oliguri med mørk urin og mindre ødemer, ofte periorbitalt. Barn utvikler tilstanden oftere enn voksne, men alle aldersgrupper kan rammes.
Akutt revmatisk feber (giktfeber) kan i sjeldne tilfeller opptre 1-5 uker etter halsbetennelse eller asymptomatisk infeksjon. Giktfeber forekommer meget sjelden hos barn under 2 år og er hyppigst i 5-10-årsalderen. Symptomer starter ofte med feber, slapphet, magesmerter og sterk svetting. Utslett og knuterosen (erythema nodosum) eller andre former for knuter i underhuden kan forekomme. Leddaffeksjon involverer vanligvis knær, håndledd, albueledd eller i ledd i foten. Leddsymptomene forsvinner etter noen dager eller uker. Alvorligere er hjerteaffeksjon, som kan involvere alle lag i hjertet å gi endokarditt, myokarditt og/eller perikarditt. Vanlige symptomer er hurtig hjerteaksjon og brystsmerter med utvikling av hjerteklaff-feil og hjertesvikt. Det kan ta flere tiår før symptomene blir alvorlig. Akutt giktfeberanfall kan vare fra uker til måneder. I forbindelse med anfall kan muskelrykninger (chorea minor) i ansikt og lemmer forekomme. Giktfeber er viktig fordi pasienter med sykdommen må få langvarig penicillinprofylakse for å unngå residiv med streptokokkinfeksjon. Residiv øker risikoen for hjerteskade. Pasienter som har hatt revmatisk endokarditt som følge av giktfeber skal ha antibiotika ved tannbehandling som involverer blødning fra tannkjøttet.
Diagnostikk
Antigen hurtigtest ved legekontor gir raske svar, men er bare beregnet på halsprøver. Antigentestene på markedet har ulik sensitivitet. I kliniske utprøvinger mot dyrkning har antigentester hatt en sensitivitet på 70-90%. Man kan som regel stole på et positivt resultat, men ikke utelukke streptokokkinfeksjon ved negativt resultat. Agenspåvisning ved dyrkning fra halsprøve gir i beste fall svar i løpet av et par døgn. I alle alvorlige tilfeller og ved residivtilfeller bør det gjøres dyrkning. Ved mistanke om immunologiske senkomplikasjoner bør det tas dyrkningsprøve av pasienten og av husstanden. Agenspåvisning i blod, spinalvæske eller annet sterilt vev eller kroppsvæske er svært viktig ved mistanke om invasiv sykdom.
Folkehelseinstituttet har referansefunksjon for Streptococcus pyogenes med hensikt å bidra til nasjonal epidemiologisk overvåking over forekomst av systemisk infeksjon, se Veileder for mikrobiologiske laboratorieanalyser. Systemiske GAS-isolat fra landets mikrobiologiske laboratorier sendes til Folkehelseinstituttet, hvor de types og oppbevares.
Ved utbrudd av skarlagensfeber eller annen GAS-infeksjon i barnehager, bør kommuneoverlege vurdere dyrkningsprøver fra noen av barna, se "Tiltak ved enkelttilfeller eller utbrudd" under.
Forekomst i Norge
Alle typer streptokokkinfeksjoner var summarisk meldingspliktig i MSIS i perioden 1975-97. I årene før meldingsplikten opphørte ble det årlig meldt cirka 40 000 tilfeller. Sepsis forårsaket av streptokokk gruppe A har vært nominativt meldingspliktig i MSIS i perioden 1975-92. Fra 1993 har alle tilfeller av alvorlig, systemisk GAS-sykdom vært meldingspliktig.
| 2014 | 2015 | 2016 | 2017 | 2018 | 2019 | 2020 | 2021 | 2022 | 2023 |
Under 1 år | 0 | 3 | 2 | 2 | 1 | 0 | 0 | 0 | 0 | 8 |
1-9 | 17 | 10 | 15 | 23 | 25 | 22 | 13 | 5 | 26 | 77 |
10-19 | 1 | 7 | 2 | 4 | 9 | 3 | 6 | 4 | 2 | 16 |
20-49 | 54 | 62 | 51 | 59 | 61 | 61 | 50 | 37 | 48 | 117 |
50-69 | 53 | 58 | 59 | 81 | 60 | 57 | 42 | 15 | 32 | 129 |
70 og over | 64 | 66 | 68 | 84 | 80 | 83 | 53 | 30 | 48 | 155 |
Totalt | 189 | 206 | 197 | 253 | 236 | 226 | 164 | 91 | 156 | 502 |
| 2019 | 2020 | 2021 | 2022 | 2023 |
Sepsis | 115 | 68 | 36 | 41 | 196 |
Nekrotiserende fasciitt | 9 | 8 | 4 | 3 | 49 |
Meningitt/Encefalitt | 1 | 1 | 0 | 1 | 4 |
Annet | 53 | 47 | 19 | 41 | 128 |
Ukjent/ikke rapportert | 57 | 47 | 33 | 73 | 156 |
Totalt | 226 | 164 | 91 | 156 | 502 |


Om GAS-situasjonen i Norge:
- Invasive infeksjoner. Årsrapport 2017
- Ukerapporter om covid-19, influensa og andre luftveisinfeksjoner
Behandling
I henhold til Retningslinjen for antibiotikabruk i primærhelsetjenesten (hdir.no) i Norge anbefales det å antibiotikabehandle moderate til alvorlige symptomgivende GAS-tonsillitter for på den måten redusere lokale, immunologiske og invasive komplikasjoner. Skarlagensfeber skal behandles med antibiotika. Les mer om antibiotikabehandling:
Det har tidvis vært mangel på en del antibiotika, særlig mikstur til barn. For oppdatert informasjon om legemiddelmangel, se:
Informasjon om bruk av antibiotikatabletter til barn:
Ved impetigo er det vanligvis tilstrekkelig med lokalbehandling, se Brennkopper. Rask sykehusinnleggelse er alltid aktuelt ved mistanke om alvorlig, invasiv infeksjon. Nekrotiserende fasciitt i underhudsvev krever øyeblikkelig operativt inngrep. Spesialisthenvisning er alltid aktuelt ved immunologiske komplikasjoner og alltid ved mistanke om giktfeber. GAS-bærerskap er vanligvis ikke indikasjon for behandling.
Forebyggende tiltak
God tildekking av sår for å unngå overføring av streptokokker ved hudinfeksjoner som brennkopper. Vanlige hygieniske tiltak som god håndvask og desinfeksjon er vesentlig, i tillegg til hostehygiene og å holde seg hjemme når man er syk. Unngå å drikke av samme flaske og glass og unngå felles bruk av samme sigarett, kluter etc. Regelmessig vask av vaskbare leker i barnehager. Det arbeides med utvikling av vaksine, men ingen vaksine er foreløpig tilgjengelig.
Tiltak ved enkelttilfelle eller utbrudd
Informasjon til pasient og pårørende om god håndhygiene og å unngå deling av glass, sigaretter og lignende. Ved et enkelttilfelle er tiltak i nærmiljøet vanligvis ikke aktuelt. Det er sjelden at sekundære, eller assosierte, tilfeller til invasiv GAS-sykdom også blir alvorlige, selv om mildere sekundærtilfeller forekommer. Ved et tilfelle av alvorlig invasiv GAS-infeksjon bør pasienten og nærkontaktene informeres om denne muligheten, slik at man eventuelt kan oppdage sykdom tidlig. Det er høyere risiko for å utvikle iGAS for eldre (over 75 år) og særlig sykehjemsbeboere, små barn (under 1 år), gravide (sent i svangerskapet og måneden etter fødsel). I tillegg kan visse kroniske sykdommer som kreft, nedsatt immunforsvar, diabetes, hjertesykdom eller samtidig infeksjon med vannkopper og influensa gi økt risiko for invasiv GAS-sykdom.
Bærerskap av GAS kan være vanskelig å utrydde med antibiotika, og bærerskap bør sjelden behandles.
Barnehager
Barn med hudinfeksjon skal behandles og holdes hjemme fra barnehagen til hudlesjoner er under kontroll (det vil si fravær av ukontrollert sekresjon, lesjoner lar seg tildekkes). Ved GAS-halsbetennelse eller ved skarlagensfeber skal barna holdes hjemme til de har vært på full antibiotikabehandling i minst ett døgn. Ubehandlet er pasienten smitteførende i cirka en uke. I tillegg må barna være klinisk friske og feberfrie. Utbrudd i barnehager med streptokokkinfeksjon er ikke uvanlig. Det er da aktuelt å informere foreldre om sykdommen og eventuelle tiltak. Forebyggende tiltak ved siden av å holde syke barn borte fra barnehagen (se over) er:
- hold barna mest mulig utendørs
- unngå blanding av barn fra ulike avdelinger i barnehagen
- vask leker og lignende daglig
- bruk kun engangshåndklær, kluter etc.
- eventuelt kan vask av felles kontaktpunkter med alkoholbasert desinfeksjonsmiddel overveies.
Bærerfrekvensen av gruppe A-streptokokker hos barna i en barnehage kan variere fra <1% til 50% avhengig av årstid og den epidemiologiske situasjonen.
Ved mistanke om GAS-sykdom hos barna bør (hals eller annen) prøve tas og behandling startes. Bærerpåvisning og ev. behandling av friske bærere i barnehager anbefales vanligvis ikke, og bør kun benyttes i unntakstilfeller ved særlig høy sykelighet, eller ved spesielt alvorlige enkelttilfeller.
Tiltak i helseinstitusjoner
Basale smittevernrutiner. Luftveisinfeksjon: Dråpesmitteregime til 1 døgn etter påbegynt effektiv antibiotikabehandling. Sårinfeksjon: Kontaktsmitteregime. Ved ikke-kontrollerbar sekresjon og ved utbredte eksfoliative hudlidelser benyttes munnbind i tillegg.
Meldings- og varslingsplikt
Meldingspliktig til MSIS kun ved systemisk eller annen alvorlig invasiv sykdom, gruppe A-sykdom. Kriterier for melding er laboratoriepåvisning av S. pyogenes fra normalt sterilt prøve-materiale ved isolering, nukleinsyre- eller antigenundersøkelse.
Normalt sterilt prøvemateriale inkluderer i denne sammenheng også kirurgisk prøvemateriale tatt med steril teknikk, f.eks. fra fascie og subkutant vev, men ikke sårsekret.
Med invasiv sykdom menes bl.a. sepsis, meningitt, barselsfeber, streptokokkal toksisk sjokksyndrom (STSS) og nekrotiserende fasciitt.
Varsling til kommuneoverlege, Folkehelseinstituttet og andre instanser ved utbrudd eller ved mistanke om overføring med næringsmidler, se Varsling av smittsomme sykdommer .
Gresk: streptos (bøyd), coccus (bær), pyon (puss), André-Alfred Lemierre (1875- 1956, Frankrike)

